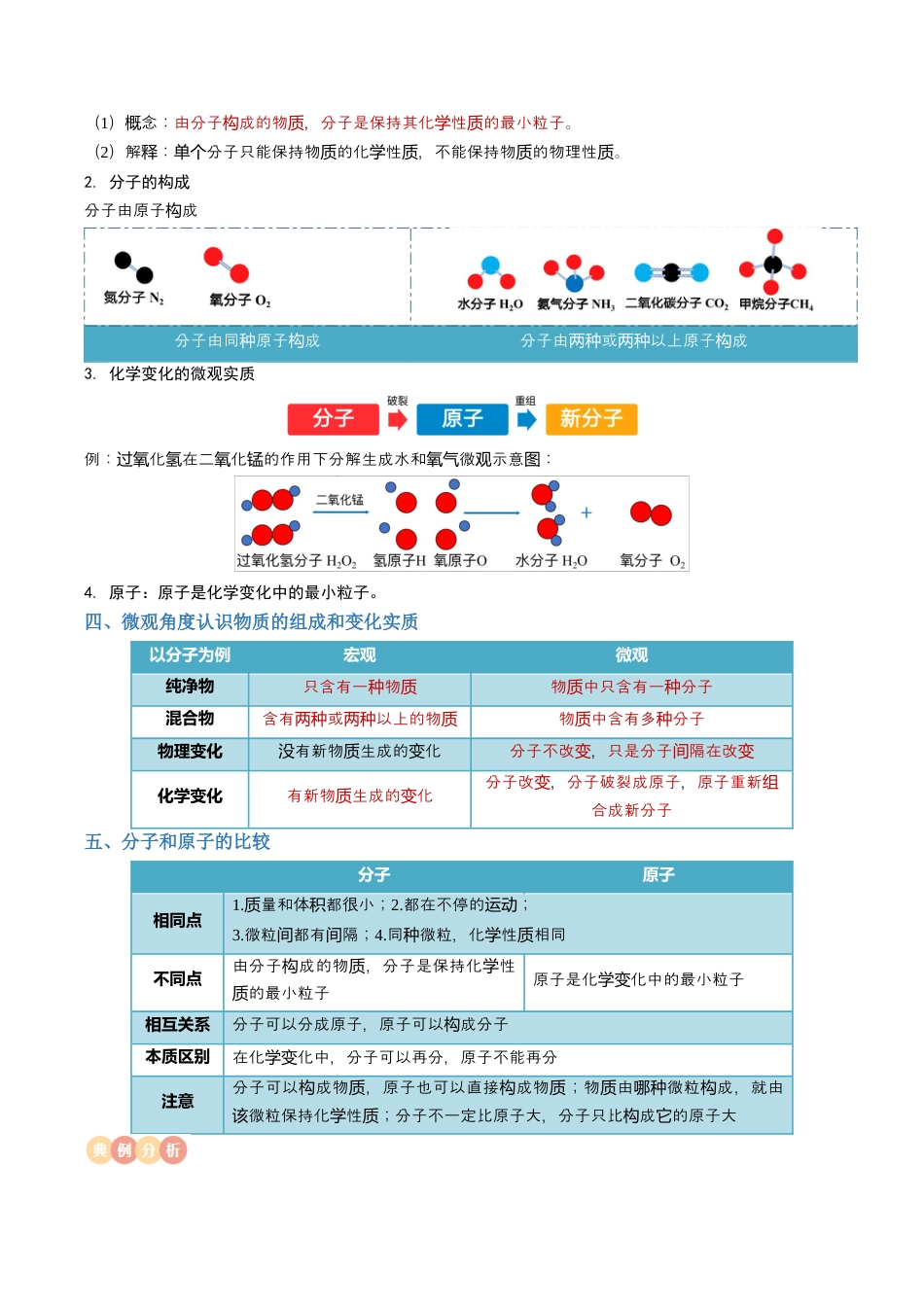
专题09物质构成的奥秘知识01分子性质知识02原子知识03离子知识04元素方法分子运动现象的探究知识01微粒(分子)性质一、物质由微粒构成物质的宏观组成和微观构成关系大多物由分子成数质构,少物由原子成数质构,一些物是由离子成的质构。例如:水由水分子成构,由原子成铁铁构,化由离子和离子成氯钠氯钠构。二、微粒的性质(以分子为例)1.分子极小,其质量和体积都很小。2.分子在不断的运动。温度越高,分子受热能量增大,运动速率加快。3.分子间有间隔(1)一般情下况,体物分子的隔比固体和液体物分子的隔相大气质间间质间间对较。(2)度升高温,分子隔增大间,度降低温,分子隔小间变。(3)强增大压,分子隔小间减,强小压减,分子隔大间变。(4)同分子成的物化性相同种构质学质,不同分子成的物化性不同种构质学质。三、分子原子定义1.分子(1)念概:由分子成的物构质,分子是保持其化性的最小粒子学质。(2)解释:分子只能保持物的化性单个质学质,不能保持物的物理性质质。2.分子的构成分子由原子成构分子由同原子成种构分子由或以上原子成两种两种构3.化学变化的微观实质例:化在二化的作用下分解生成水和微示意过氧氢氧锰氧气观图:4.原子:原子是化学变化中的最小粒子。四、微观角度认识物质的组成和变化实质以分子为例宏观微观纯净物只含有一物种质物中只含有一分子质种混合物含有或以上的物两种两种质物中含有多分子质种物理变化有新物生成的化没质变分子不改变,只是分子隔在改间变化学变化有新物生成的化质变分子改变,分子破裂成原子,原子重新组合成新分子五、分子和原子的比较分子原子相同点1.量和体都很小质积;2.都在不停的运动;3.微粒都有隔间间;4.同微粒种,化性相同学质不同点由分子成的物构质,分子是保持化性学的最小粒子质原子是化化中的最小粒子学变相互关系分子可以分成原子,原子可以成分子构本质区别在化化中学变,分子可以再分,原子不能再分注意分子可以成物构质,原子也可以直接成物构质;物由微粒成质哪种构,就由微粒保持化性该学质;分子不一定比原子大,分子只比成的原子大构它【例1】(2023·山东泰安·统考中考真题)对下列事实的解释不合理的是()A.通过气味区别氮气和氨气——分子是运动的,不同分子的性质不同B.干冰升华为二氧化碳气体——状态变化,分子大小随之变化C.氧气经压缩储存在钢瓶中——压强增大,分子之间的间隔变小D.蔗糖在热水中溶解更快——温度升高分子的运动速率加快【答案】B【详解】A、通过气味区别氮气和氨气,是因为分子是不断运动的,氮分子和氨分子不断运动,运动到人的鼻孔中,由于不同分子性质不同,氮气是无味的,氨气有刺激性气味,气味不同,故可以区分,不符合题意;B、干冰升华为二氧化碳气体,是因为状态改变,分子之间的间隔改变,分子的大小不变,符合题意;C、氧气经压缩储存在钢瓶中,是因为分子之间存在间隔,压强增大,分子之间的间隔变小,不符合题意;D、蔗糖在热水中溶解更快,是因为分子在不断运动,温度越高,分子的运动速率越快,不符合题意。故选B。知识02原子一、原子的构成原子中,原子核位于原子中心,原子的量主要集中在原子核上质,原子核由子和中子成质构。1.原子核带正电,原子核带的正电荷数(即核电荷数)与核外电子带的负电荷数(数值上等于核外电子数)相等,电性相反,所以原子不显电性。2.原子中的等量关系:核电荷数=质子数=核外电子数二、原子核外电子排布1.核外电子排布规律第1最多容层纳2子,第个电2最多容层纳8子。个电最外子不超层电数过8(只有个1的,子不超层电过2)个2.原子结构示意图3.原子结构排布规律:每一排,子相同,最外子左到右依次增横电层数层电数从递;除稀有体外气,每一列,最外子相同,子上到下依次增纵层电数电层数从递。三、原子结构和元素的化学性质关系最外子定化性层电数决学质,最外子相同化性一般相似层电数学质。【注意】原子最外氦层2子个电,但于相定属对稳结构,最外与层8子的稀有体原子化性相个电气学质似,最外与层2子的其他原子化性不相似个电学质。四、相对原子质量1.概念:以一种碳原子质量的1/12(1.66×10-27kg)为标准...