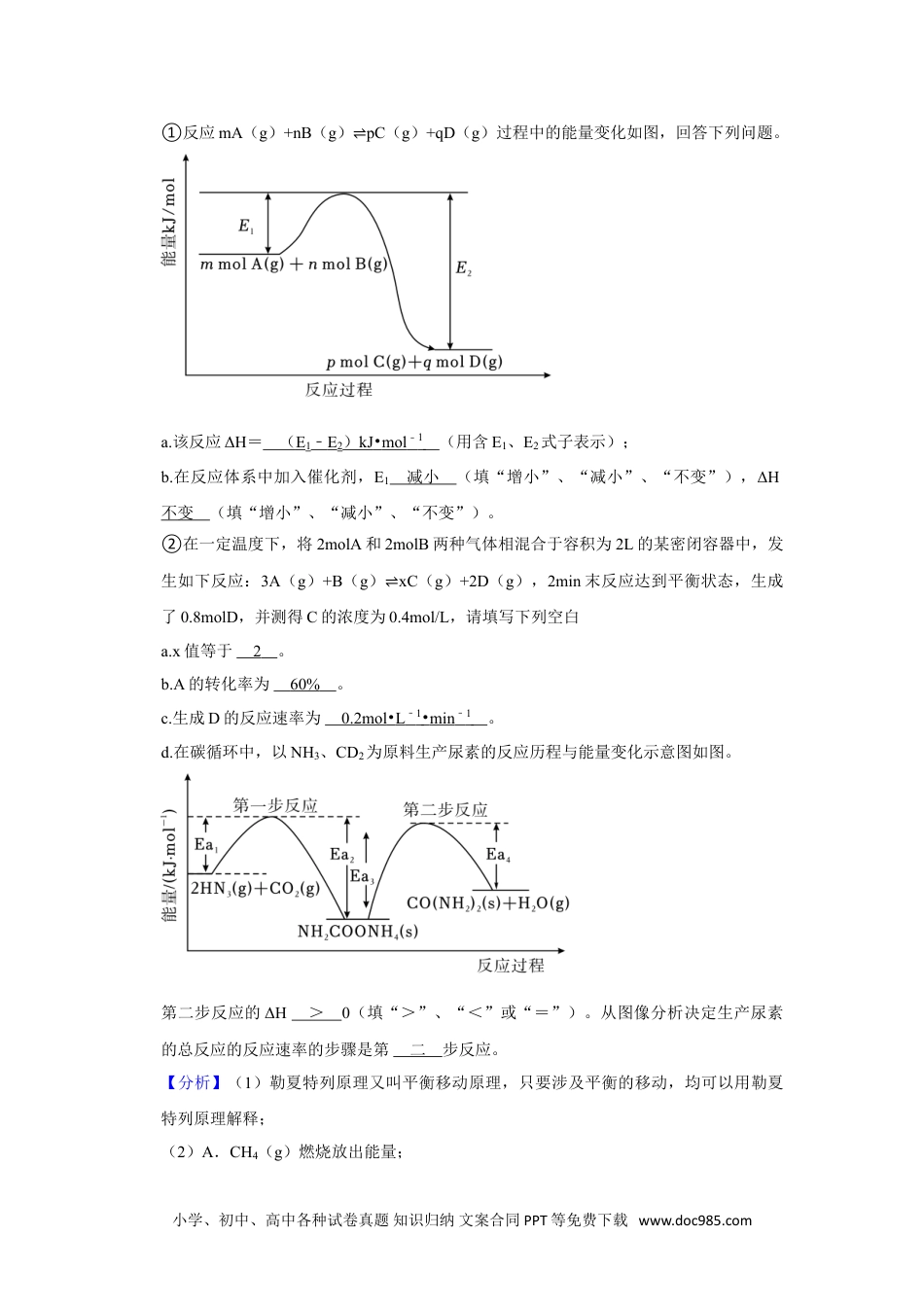
2023-2024学年上海市嘉定区高三(上)期末化学试卷(一模)参考答案与试题解析一.阅读下列材料,完成以下问题(13分)1.(13分)化学反应千千万万,我们日常生活中天天都会发生。但是深入研究后,我们会发现其实化学反应也是有它的本质的,实质就是分子之间的碰撞,于是就会有速率和温度的说法。(1)下列事实不能用化学平衡移动原理解释的是C。A.实验室收集氯气时,常用排饱和食盐水的方法B.用浓氨水和氢氧化钠固体快速制取氨气C.工业合成氨N2(g)+3H2(g)⇌2NH3(g)ΔH<0,采用400℃~500℃的高温条件D.红棕色NO2加压后颜色先变深后变浅(2)下列热化学方程式书写正确的是D。A.CH4(g)燃烧的热化学方程式:CH4(g)+2O2(g)=CD2(g)+2H2O(l)ΔH=890.3kJ•mol﹣1B.2NO2=O2+2NOΔH=+116.2kJ•mol﹣1C.一定条件下,0.5molH2与1molI2(g)充分反应生成HI(g)放热akJ,其热化学方程式为:H2(g)+I2(g)=2HI(g)ΔH=﹣2akJ•mol﹣1D.已知:1molH2(g)与1molCl2(g)反应生成2molHCl(g)时,放出184.6kJ的热量,则有:H2(g)+Cl2(g)=HCl(g)ΔH=﹣92.3kJ•mol﹣1(3)(双选)羰基硫(CDS)可作为一种粮食熏蒸剂,能防止某些昆虫、线虫和真菌的危害。在恒容密闭容器中,将CD和H2S混合加热并达到下列平衡:CD(g)+H2S(g)⇌CDS(g)+H2(g)K=0.1.反应前CD的物质的量为10mol,平衡后CD的物质的量为8mol。下列说法正确的是CD。A.升高温度,H2S浓度增小,表明该反应是吸热反应B.通入CD,正反应速率逐渐增小C.反应前H2S的物质的量为7molD.CD的平衡转化率为20%(4)按要求完成下列问题。小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com①反应mA(g)+nB(g)⇌pC(g)+qD(g)过程中的能量变化如图,回答下列问题。a.该反应ΔH=(E1﹣E2)kJ•mol﹣1(用含E1、E2式子表示);b.在反应体系中加入催化剂,E1减小(填“增小”、“减小”、“不变”),ΔH不变(填“增小”、“减小”、“不变”)。②在一定温度下,将2molA和2molB两种气体相混合于容积为2L的某密闭容器中,发生如下反应:3A(g)+B(g)⇌xC(g)+2D(g),2min末反应达到平衡状态,生成了0.8molD,并测得C的浓度为0.4mol/L,请填写下列空白a.x值等于2。b.A的转化率为60%。c.生成D的反应速率为0.2mol•L﹣1•min﹣1。d.在碳循环中,以NH3、CD2为原料生产尿素的反应历程与能量变化示意图如图。第二步反应的ΔH>0(填“>”、“<”或“=”)。从图像分析决定生产尿素的总反应的反应速率的步骤是第二步反应。【分析】(1)勒夏特列原理又叫平衡移动原理,只要涉及平衡的移动,均可以用勒夏特列原理解释;(2)A.CH4(g)燃烧放出能量;小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.comB.2NO2=O2+2NOΔH=+116.2kJ•mol﹣1,该方程式中物质的聚集状态未标出;C.一定条件下,0.5molH2与1molI2(g)充分反应生成HI(g)放热akJ,该反应为可逆反应,完全反应放出的热量小于akJ;D.已知:1molH2(g)与1molCl2(g)反应生成2molHCl(g)时,放出184.6kJ的热量,物质的量减半,则焓变减半;(3)在恒容密闭容器中,将CD和H2S混合加热并达到下列平衡,反应前CD的物质的量为10mol,平衡后CD的物质的量为8mol,则假设的起始物质的量为x,列出三段式结合化学平衡常数K=解得硫化氢的初始投料量和CD的平衡转化率,A.升高温度,H2S浓度增小,表明平衡逆向移动,逆向吸热;B.通入CD,正反应速率突然增小,后逐渐减小;C.有以上三段式可知,反应前H2S的物质的量;D.有以上三段式分析可知,CD的平衡转化率;(4)①a.该反应ΔH=正反应的活化能﹣逆反应的活化能;b.在反应体系中加入催化剂,正、逆反应活化能均减小,但对焓变不会影响;②a.在一定温度下,将2molA和2molB两种气体相混合于容积为2L的某密闭容器中,发生如下反应:3A(g)+B(g)⇌xC(g)+2D(g),2min末反应达到平衡状态,生成了0.8molD,并测得C的浓度为0.4mol/L,则生成C的物质的量为0.4mol/L×2L=0.8mol,列出三段式解得x=2;b.依据三段式解得A的转化率;c.依...