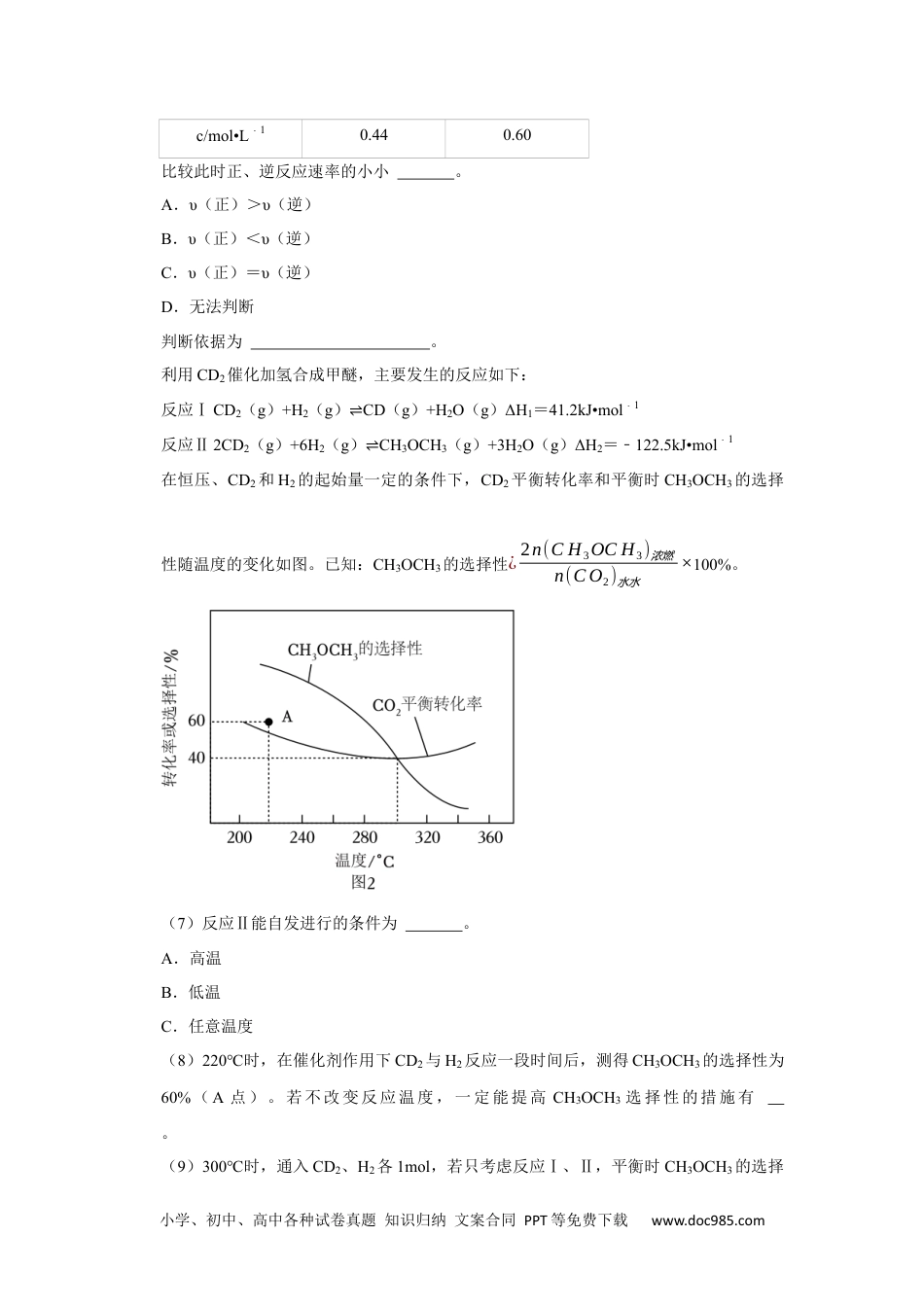
小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com2023-2024学年上海市徐汇区高三(上)期末化学试卷(一模)一、清洁燃料1.(25分)甲醚(CH3OCH3)是一种重要的清洁燃料,未来可能替代柴油和液化气作为洁净燃料使用。(1)乙醇也是一种清洁燃料,乙醇的沸点为78.5℃,而甲醚的沸点为﹣23℃,解释沸点差异的原因。(2)下列工业中以提高汽油、柴油等轻质液体燃料的产量和质量为目的是。A.石油分馏B.重油裂解C.石油裂化D.煤的干馏利用水煤气合成甲醚的三步反应如下:①2H2(g)+CD(g)⇌CH3OH(g)ΔH1=﹣90.8kJ•mol1﹣②2CH3OH(g)⇌CH3OCH3(g)+H2O(g)ΔH2=﹣23.5kJ•mol1﹣③CD(g)+H2O(g)⇌CD2(g)+H2(g)ΔH3=﹣41.2kJ•mol1﹣(3)总反应:3H2(g)+3CD(g)⇌CH3OCH3(g)+CD2(g)ΔH=。(4)一定条件下,起始浓度分别为c(CD)=0.6mol•L1﹣、c(H2)=1.4mol•L1﹣,8min后反应①达到化学平衡,CD的平衡转化率为50%,则8min内H2的平均反应速率为。(5)一定温度下,在恒容密闭容器中发生反应②,当容器内气体的总压强不再变化时。下列说法正确的是。A.该反应可能处于化学平衡状态B.正、逆反应速率一定相等C.CH3OH全部转化为CH3OCH3和H2OD.CH3OH、CH3OCH3、H2O的浓度一定相等(6)T℃时,反应②的平衡常数为2。此温度下,向密闭容器中加入一定量的CH3OH,某时刻测得部分组分的浓度如下:物质CH3OHCH3OCH3小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.comc/mol•L1﹣0.440.60比较此时正、逆反应速率的小小。A.υ(正)>υ(逆)B.υ(正)<υ(逆)C.υ(正)=υ(逆)D.无法判断判断依据为。利用CD2催化加氢合成甲醚,主要发生的反应如下:反应ⅠCD2(g)+H2(g)⇌CD(g)+H2O(g)ΔH1=41.2kJ•mol1﹣反应Ⅱ2CD2(g)+6H2(g)⇌CH3OCH3(g)+3H2O(g)ΔH2=﹣122.5kJ•mol1﹣在恒压、CD2和H2的起始量一定的条件下,CD2平衡转化率和平衡时CH3OCH3的选择性随温度的变化如图。已知:CH3OCH3的选择性¿2n(CH3OCH3)浓燃n(CO2)水水×100%。(7)反应Ⅱ能自发进行的条件为。A.高温B.低温C.任意温度(8)220℃时,在催化剂作用下CD2与H2反应一段时间后,测得CH3OCH3的选择性为60%(A点)。若不改变反应温度,一定能提高CH3OCH3选择性的措施有。(9)300℃时,通入CD2、H2各1mol,若只考虑反应Ⅰ、Ⅱ,平衡时CH3OCH3的选择小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com性、CD2的平衡转化率均为40%,平衡时生成CH3OCH3的物质的量为mol。(10)温度高于300℃时,CD2平衡转化率随温度升高而增加的原因是。(11)以甲醚、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池。该电池负极的电极反应为。二、金属冶炼2.(25分)金属铜被广泛应用于电气、电子等领域。因原料和工艺不同,铜的冶炼主要有火法冶炼与湿法冶炼两种技术路线。(1)铜元素位于元素周期表的。A.s区B.p区C.ds区D.f区(2)基态Cu原子的核外电子排布式。火法冶炼是以黄铜矿(CuCES2)为主要原料,如图是一种火法制备高纯度铜的工艺。(3)黄铜矿熔炼过程中会发生反应:2CuCES2+O2=Cu2S+2CES+SO2。若2molCuCES2参与反应,转移电子数目为。在上述反应中,SO2是。(不定项)A.氧化剂B.还原剂C.还原产物D.氧化产物(4)吹炼过程中,向熔融的冰铜中加入SiO2的目的是。(5)粗铜经电解精炼可获得高纯度铜,下列说法正确的是。A.粗铜做阴极,发生氧化反应小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.comB.电解质溶液中铜离子向阴极移动C.利用阳极泥可回收Ag、Zn、Au等金属D.当电路中通过的电子数为NA时,阳极的质量变化一定是32g(6)关于SO2的说法正确的是。(不定项)A.中心原子的杂化类型为sp2B.电负性:O<SC.属于非极性分子D.价层电子对的空间结构为平面三角形(7)煤中掺入一定量的生石灰,能减少煤燃烧排放的SO2,体现SO2具有。A.漂白性B.酸性氧化物的性质C.氧化性D.还原性(8)冶铜烟气可以作为工业制硫酸为原料。下列的说法正确的是。A...