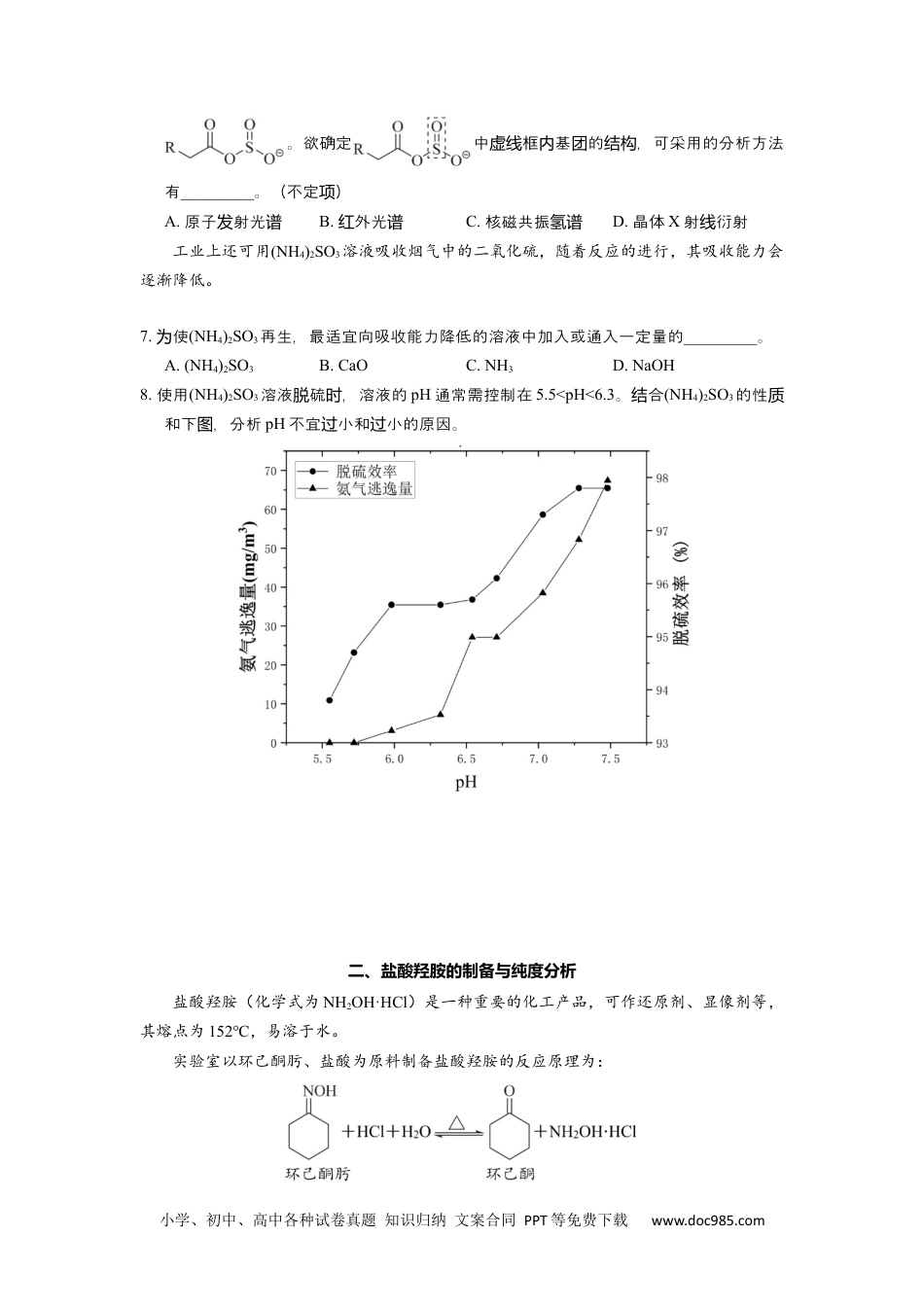
小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com嘉定区2022~2023学年第一学期期末质量监控试卷高三化学2023.12考生注意:1.卷分试满100分,考试时间60分。钟2.本考分卷和答。答前,必在答上姓名、考。试设试题纸题务题纸填写号3.作答必按位置涂或在答上,在卷上作答一律不得分。须对应写题纸试4.注“标不定项”的,每小有试题题1~2个符合件的。条选项相原子量:对质H-1C-12N-14O-16Cl-35.5CE-56一、工业烟气脱硫的方法工业排放的某些烟气中含有二氧化硫等小气污染物,对其进行脱硫治理不仅可以防止有害物质排放,还可以生产其他有用的产品。1.SO2分子的空和间结构分子的性分极别为_________。A.直形,非性线极B.直形,性线极C.角形,非性极D.角形,性极2.第一离能:电P>S,合核外子排布相知,明其原因。结电关识说沿海地区的某煤电厂开发出海水脱硫的新工艺,流程如下图所示:25℃时H2SO3、H2CD3的电离常数如下表所示:弱酸Ka1Ka2H2SO31.3×10-26.2×10-8H2CD34.5×10-74.7×10-113.在吸收塔,烟吸收塔的内气应从_________通入,塔淋的海水充分接。与顶喷触A.上部B.中部C.下部4.吸收塔度不宜高,原因可能是内温过_____________________________________________。(列举1)条吸收塔内SO2和海水中HCD3-生反的离子方程式发应为___________________________。5.若煤排放烟量电厂气为2.0×106kg⋅h-1,其中含SO2为0.15%,烟海水硫理后该气经脱处SO2为144kg⋅h-1,硫率则脱=_________。(硫率脱)6.离子液体(ILs)也可以用理工烟。来处业气ILs的离子吸收负SO2后生成小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com。欲确定中框基的,可采用的分析方法虚线内团结构有_________。(不定)项A.原子射光发谱B.外光红谱C.核磁共振氢谱D.晶体X射衍射线工业上还可用(NH4)2SO3溶液吸收烟气中的二氧化硫,随着反应的进行,其吸收能力会逐渐降低。7.使为(NH4)2SO3再生,最适宜向吸收能力降低的溶液中加入或通入一定量的_________。A.(NH4)2SO3B.CaOC.NH3D.NaOH8.使用(NH4)2SO3溶液硫,溶液的脱时pH通常需控制在5.5<pH<6.3。合结(NH4)2SO3的性质和下,分析图pH不宜小和小的原因。过过二、盐酸羟胺的制备与纯度分析盐酸羟胺(化学式为NH2OH·HCl)是一种重要的化工产品,可作还原剂、显像剂等,其熔点为152℃,易溶于水。实验室以环己酮肟、盐酸为原料制备盐酸羟胺的反应原理为:小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com制备盐酸羟胺的实验装置如图所示(加热、搅拌和夹持装置已省略)。盐酸羟胺在不同温度下的溶解度如下表:温度(℃)溶解度(g/100gH2O)2046.74054.96063.28071.19.器甲中水口仪进应为_________。A.a处B.b处C.a或处b均可处10.反程中,己不蒸出的主要原因是应过将环酮断____________________________________。11.容器乙中收集到己的水溶液,己和水之存在的相互作用有环酮环酮间_________。(不定)项A.共价键B.离子键C.氢键D.范德力华12.反后,三口的溶液中取酸的方法应从烧瓶获盐羟胺实验为_________。A.冷却晶结B.渗析C.蒸馏D.萃取、分液称取0.500g由上述方法制得的盐酸羟胺产品,加水配制成100mL溶液。量取20.00mL于锥形瓶中,加入适量稀硫酸酸化,再加入过量硫酸铁铵[NH4CE(SO4)2]溶液充分反应,接着加入足量磷酸溶液(与CE3+形成无色配合物),最后用0.0500mol⋅L-1KMnO4的酸性溶液滴定,达到滴定终点时消耗KMnO4的酸性溶液的体积为11.35mL。反应原理为:①NH2OH·HCl⇌NH2OH+HCl②2NH2OH+4CE3+=4CE2++______+______+H2O③MnO4-+5CE2++8H+=5CE3++Mn2++4H2O13.反②充完整,出子移的方向和目。将应补并标电转数14.配制上述酸溶液所需要的定量器有盐羟胺仪_________。(不定)项A.子天平电B.100mL容量瓶C.滴定管D.量筒判滴定点的象断终现为______________________________________________________。15.通算判品的度。(出算程)过计断该产纯级别写计过度纯级别优级纯分析纯化学纯量分质数ω(NH2OH·HCl)/%≥99.0≥98.5≥97.0已知:M(NH2OH·HCl)=69.5g·mol-1小学、初中、高中各种试卷...