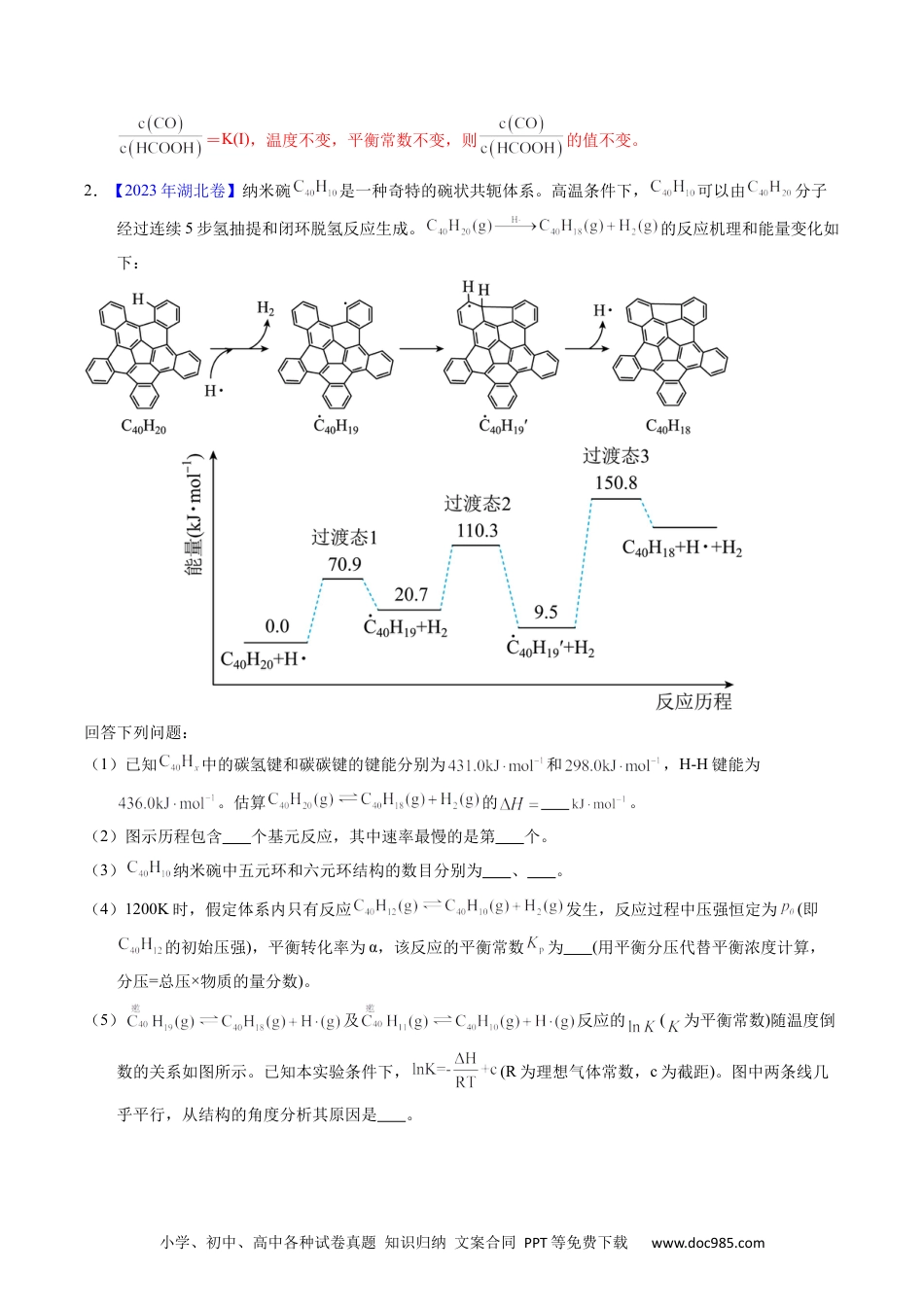
小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com1.【2023年山东卷】一定条件下,水气变换反应的中间产物是。为探究该反应过程,研究水溶液在密封石英管中的分子反应:Ⅰ.Ⅱ.研究发现,在反应Ⅰ、Ⅱ中,仅对反应Ⅰ有催加速作用;反应Ⅰ速率远大于反应Ⅱ,近似认为反应Ⅰ建立平衡后始终处于平衡状态。忽略水电离,其浓度视为常数。回答下列问题:(1)一定条件下,反应Ⅰ、Ⅱ的焓变分别为、,则该条件下水气变换反应的焓变(用含的代数式表示)。(2)反应Ⅰ正反应速率方程为:,k为反应速率常数。温度下,电离平衡常数为,当平衡浓度为时,浓度为,此时反应Ⅰ应速率(用含和k的代数式表示)。(3)温度下,在密封石英管内完全充满水溶液,使分解,分解产物均完全溶于水。含碳物种浓度与反应时间的变化关系如图所示(忽略碳元素的其他存在形式)。时刻测得的浓度分别为,反应Ⅱ达平衡时,测得的浓度为。体系达平衡后(用含y的代数式表示,下同),反应Ⅱ的平衡常数为。相同条件下,若反应起始时溶液中同时还含有盐酸,则图示点中,的浓度峰值点可能是(填标号)。与不同盐酸相比,达浓度峰值时,浓度(填“增大”“减小”或“不变”),的反应(填“增大”“减小”或“不变”)。专题65原理合——反综题应热+速率+平衡小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com【答案】(1)-(2)(3)a减小不变【解析】(1)根据盖斯定律,反应II-反应I=水气变换反应,故水气变换反应的焓变=-;(2)T1温度时,HCOOH建立电离平衡:,c(HCOO-)=c(H+),故c(H+)=。。(3)t1时刻时,c(CO)达到最大值,说明此时反应I达平衡状态。此时故t1时刻c(HCOOH)=1.0-0.70-0.16=0.14mol·L-1,K(I)=。t1时刻→反应II达平衡过程,则c(H2)=b+0.16=y,b=(y-0.16)mol·L-1,c(HCOOH)=0.14-a-b=0.3-a-y,c(CO)=a+0.7,K(I)=,a=。故=,K(II)=。加入0.1mol·L-1盐酸后,H+对反应I起催化作用,加快反应I的反应速率,缩短到达平衡所需时间,故CO浓度峰值提前,由于时间缩短,反应Ⅱ消耗的HCOOH减小,体系中HCOOH浓度增大,导致CO浓度大于t1时刻的峰值,故c(CO)最有可能在a处达到峰值。此时c(CO2)会小于不含盐酸的浓度,小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com=K(I),温度不变,平衡常数不变,则的值不变。2.【2023年湖北卷】纳米碗是一种奇特的碗状共轭体系。高温条件下,可以由分子经过连续5步氢抽提和闭环脱氢反应生成。的反应机理和能量变化如下:回答下列问题:(1)已知中的碳氢键和碳碳键的键能分别为和,H-H键能为。估算的。(2)图示历程包含个基元反应,其中速率最慢的是第个。(3)纳米碗中五元环和六元环结构的数目分别为、。(4)1200K时,假定体系内只有反应发生,反应过程中压强恒定为(即的初始压强),平衡转化率为α,该反应的平衡常数为(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。(5)及反应的(为平衡常数)随温度倒数的关系如图所示。已知本实验条件下,(R为理想气体常数,c为截距)。图中两条线几乎平行,从结构的角度分析其原因是。小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com(6)下列措施既能提高反应物的平衡转化率,又能增大生成的反应速率的是(填标号)。a.升高温度b.增大压强c.加入催化剂【答案】(1)128(2)33(3)610(4)(5)在反应过程中,断裂和形成的化学键相同(6)a【解析】(1)由和的结构式和反应历程可以看出,中断裂了2根碳氢键,形成了1根碳碳键,所以的=,故答案为:128;(2)由反应历程可知,包含3个基元反应,分别为:,,,其中第三个的活化能最大,反应速率最慢,故答案为:3;3;(3)由的结构分析,可知其中含有1个五元环,10个六元环,每脱两个氢形成一个五元环,则总共含有6个五元环,10个六元环,故答案为:6;10;(4)1200K时,假定体系内只有反应发生,反应过程中压强恒定为(即的初始压强),平衡转化率为α,设起始量为1mol,则根据信息列出三段式为:小学、初中、高中各种试卷真题知识归纳...