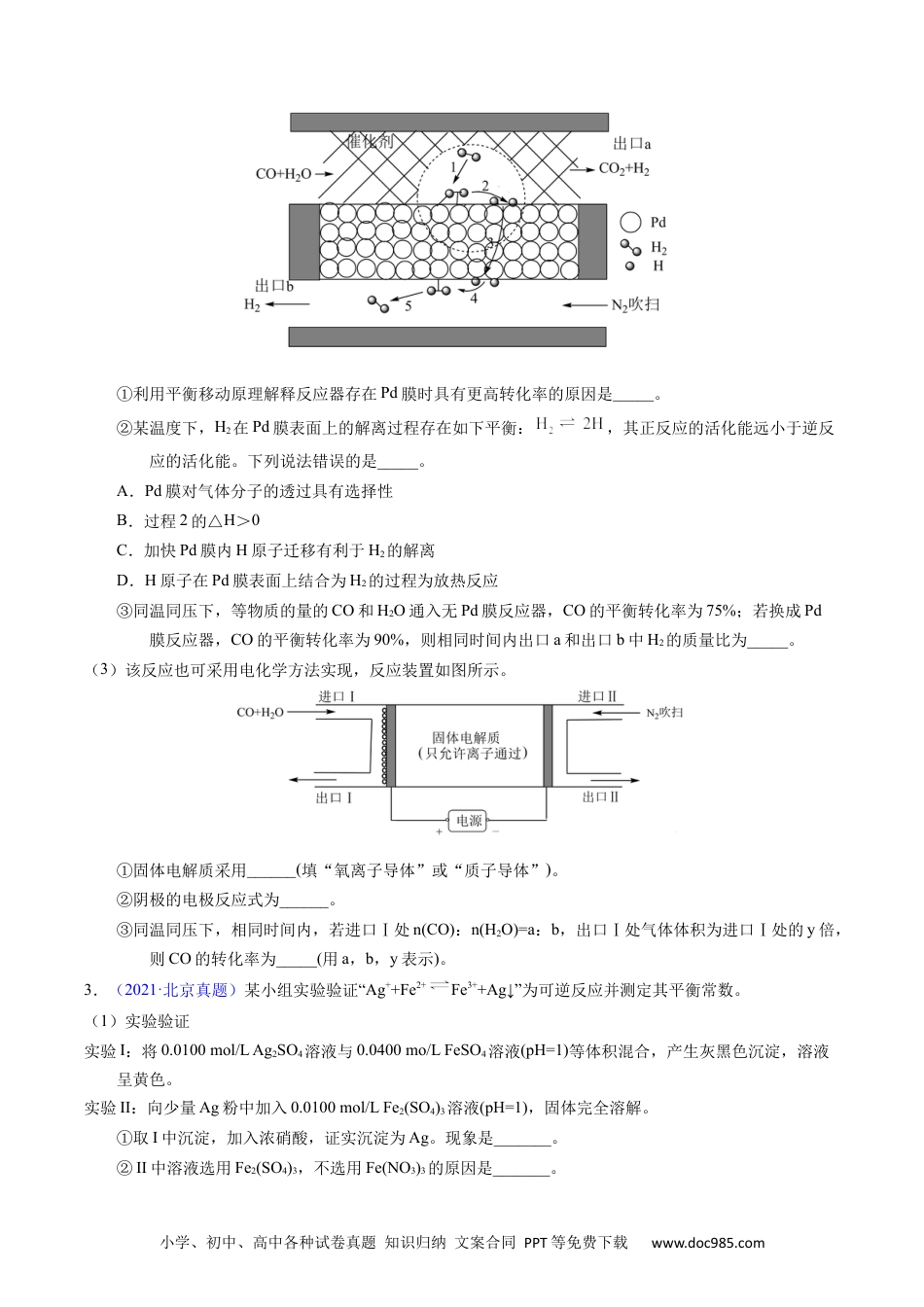
小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com1.【2023年北京卷】尿素合成的发展体现了化学科学与技术的不断进步。(1)十九世纪初,用氰酸银与在一定条件下反应制得,实现了由无机物到有机物的合成。该反应的化学方程式是。(2)二十世纪初,工业上以和为原料在一定温度和压强下合成尿素。反应分两步:ⅰ.和生成;ⅱ.分解生成尿素。结合反应过程中能量变化示意图,下列说法正确的是(填序号)。a.活化能:反应ⅰ<反应ⅱb.ⅰ为放热反应,ⅱ为吸热反应c.(3)近年研究发现,电催化和含氮物质(等)在常温常压下合成尿素,有助于实现碳中和及解决含氮废水污染问题。向一定浓度的溶液通至饱和,在电极上反应生成,电解原理如图所示。专题66原理合综题——反应热+速率+平衡+化电学小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com①电极是电解池的极。②电解过程中生成尿素的电极反应式是。(4)尿素样品含氮量的测定方法如下。已知:溶液中不能直接用溶液准确滴定。①消化液中的含氮粒子是。②步骤ⅳ中标准溶液的浓度和消耗的体积分别为和,计算样品含氮量还需要的实验数据有。2.【2022年重庆卷】反应在工业上有重要应用。(1)该反应在不同温度下的平衡常数如表所示。温度/℃7008008301000平衡常数1.671.11.000.59①反应的△H_____0(填“>”“<”或“=”)。②反应常在较高温度下进行,该措施的优缺点是_____。(2)该反应常在Pd膜反应器中进行,其工作原理如图所示。小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com①利用平衡移动原理解释反应器存在Pd膜时具有更高转化率的原因是_____。②某温度下,H2在Pd膜表面上的解离过程存在如下平衡:,其正反应的活化能远小于逆反应的活化能。下列说法错误的是_____。A.Pd膜对气体分子的透过具有选择性B.过程2的△H>0C.加快Pd膜内H原子迁移有利于H2的解离D.H原子在Pd膜表面上结合为H2的过程为放热反应③同温同压下,等物质的量的CO和H2O通入无Pd膜反应器,CO的平衡转化率为75%;若换成Pd膜反应器,CO的平衡转化率为90%,则相同时间内出口a和出口b中H2的质量比为_____。(3)该反应也可采用电化学方法实现,反应装置如图所示。①固体电解质采用______(填“氧离子导体”或“质子导体”)。②阴极的电极反应式为______。③同温同压下,相同时间内,若进口Ⅰ处n(CO):n(H2O)=a:b,出口Ⅰ处气体体积为进口Ⅰ处的y倍,则CO的转化率为_____(用a,b,y表示)。3.(2021·北京真题)某小组实验验证“Ag++Fe2+Fe3++Ag↓”为可逆反应并测定其平衡常数。(1)实验验证实验I:将0.0100mol/LAg2SO4溶液与0.0400mo/LFeSO4溶液(pH=1)等体积混合,产生灰黑色沉淀,溶液呈黄色。实验II:向少量Ag粉中加入0.0100mol/LFe2(SO4)3溶液(pH=1),固体完全溶解。①取I中沉淀,加入浓硝酸,证实沉淀为Ag。现象是_______。②II中溶液选用Fe2(SO4)3,不选用Fe(NO3)3的原因是_______。小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com综合上述实验,证实“Ag++Fe2+Fe3++Ag↓”为可逆反应。③小组同学采用电化学装置从平衡移动角度进行验证。补全电化学装置示意图,写出操作及现象_______。(2)测定平衡常数实验Ⅲ:一定温度下,待实验Ⅰ中反应达到平衡状态时,取vmL上层清液,用c1mol/LKSCN标准溶液滴定Ag+,至出现稳定的浅红色时消耗KSCN标准溶液v1mL。资料:Ag++SCN-AgSCN↓(白色)K=1012Fe3++SCN-FeSCN2+(红色)K=102.3①滴定过程中Fe3+的作用是_______。②测得平衡常数K=_______。(3)思考问题①取实验I的浊液测定c(Ag+),会使所测K值_______(填“偏高”“偏低”或“不受影响”)。②不用实验II中清液测定K的原因是_______。4.【2021年重庆卷】含结晶水的无机物可应用在吸波材料、电极材料和相变储能材料等领域。胆矾(CuSO4·5H2O)是一种重要的结晶水合物。(1)硫酸铜参比电极具有电位稳定的优点,可用于土壤环境中钢质管道的电位监测。测量的电化学原理如图所示。回答下列问题:小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.d...