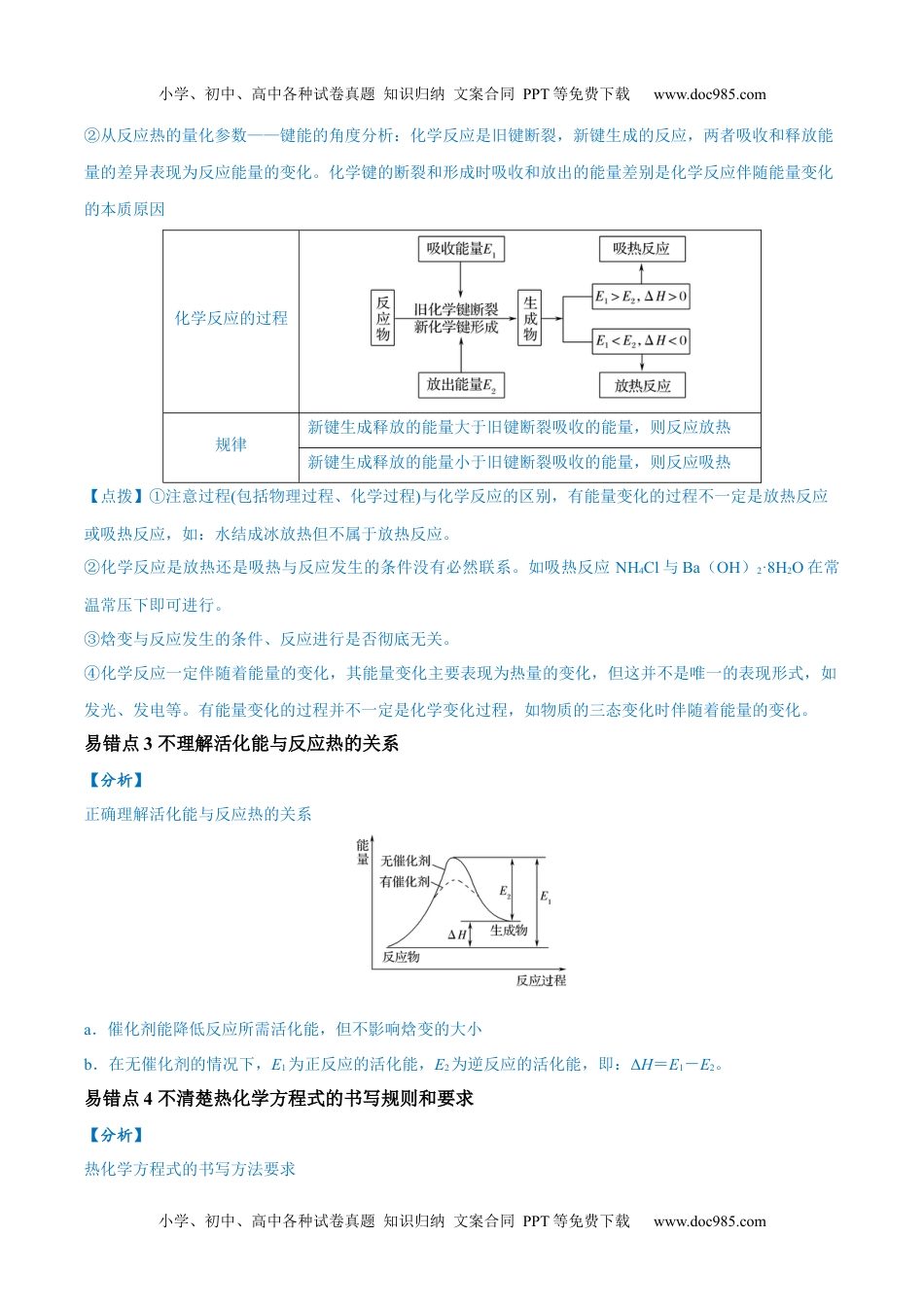
小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com易错类型10化学能与热能易错点1不清楚能量高低与物质稳定性的关系易错点2化学反应过程吸放热的判断易错点3不理解活化能与反应热的关系易错点4不清楚热化学方程式的书写规则和要求易错点5不清楚反应热、燃烧热和中和热的区别和联系易错点6不会根据化学键键能计算ΔH易错点7不会进行反应热的大小比较易错点8不会利用盖斯定律进行反应热的计算易错点9不会分析反应历程、机理图易错点1不清楚能量高低与物质稳定性的关系【分析】能量越低越稳定。同一物质能量由高到低:气体(g)>液体(l)>固体(s);稳定性:气体(g)<液体(l)<固体(s)易错点2化学反应过程吸放热的判断【分析】放热反应和吸热反应(1)化学反应放热和吸热的原因①从反应物和生成物的总能量相对大小的角度分析图示结论反应物的总能量大于生成物的总能量为放热反应,即:E(反应物)>E(生成物)反应物的总能量小于生成物的总能量为吸热反应,即:E(反应物)<E(生成物)小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com②从反应热的量化参数——键能的角度分析:化学反应是旧键断裂,新键生成的反应,两者吸收和释放能量的差异表现为反应能量的变化。化学键的断裂和形成时吸收和放出的能量差别是化学反应伴随能量变化的本质原因化学反应的过程规律新键生成释放的能量大于旧键断裂吸收的能量,则反应放热新键生成释放的能量小于旧键断裂吸收的能量,则反应吸热【点拨】①注意过程(包括物理过程、化学过程)与化学反应的区别,有能量变化的过程不一定是放热反应或吸热反应,如:水结成冰放热但不属于放热反应。②化学反应是放热还是吸热与反应发生的条件没有必然联系。如吸热反应NH4Cl与Ba(OH)2·8H2O在常温常压下即可进行。③焓变与反应发生的条件、反应进行是否彻底无关。④化学反应一定伴随着能量的变化,其能量变化主要表现为热量的变化,但这并不是唯一的表现形式,如发光、发电等。有能量变化的过程并不一定是化学变化过程,如物质的三态变化时伴随着能量的变化。易错点3不理解活化能与反应热的关系【分析】正确理解活化能与反应热的关系a.催化剂能降低反应所需活化能,但不影响焓变的大小b.在无催化剂的情况下,E1为正反应的活化能,E2为逆反应的活化能,即:ΔH=E1-E2。易错点4不清楚热化学方程式的书写规则和要求【分析】热化学方程式的书写方法要求小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com(1)遵循一般化学方程式的书写规则,一般不写反应条件,不标气体和沉淀符号。(2)标注ΔH的正负。化学方程式后面空一格标注ΔH,若为放热反应,ΔH为“-”;若为吸热反应,ΔH为“+”。(3)计算ΔH的数值和单位。根据化学方程式中的化学计量数计算写出ΔH的数值。ΔH单位是kJ·mol-1。(4)标注各物质的聚集状态。在物质后面用括号标注各物质的聚集状态:气体用“g”,液体用“l”,固体用“s”,溶液用“aq”。(5)标注反应的温度和压强。没有特殊说明是指25℃、101kPa,该条件可以不标注,但其他条件必须标注。(6)热化学方程式中各物质化学式前的化学计量数只表示其物质的量,可以是整数或分数。(7)热化学方程式中化学式前面的化学计量数必须与ΔH相对应,若化学计量数加倍,则ΔH的数值也要加倍。如:H2(g)+O2(g)===H2O(l)ΔH=-285.8kJ·mol-12H2(g)+O2(g)===2H2O(l)ΔH=-571.6kJ·mol-1(8)逆反应的ΔH数值与正反应的相等、符号相反。【点拨】①热化学方程式中不用标明反应条件(如“加热”“高温”“催化剂”等)。②热化学方程式中不再用“↑”、“↓”来标记气体生成物和难溶生成物。③热化学方程式中一般用“===”、可逆反应中用“”,即便是有机反应的热化学方程式中也不用“”。④由于同素异形体的结构不同,所以焓不同,故化学式相同的不同单质与相同...