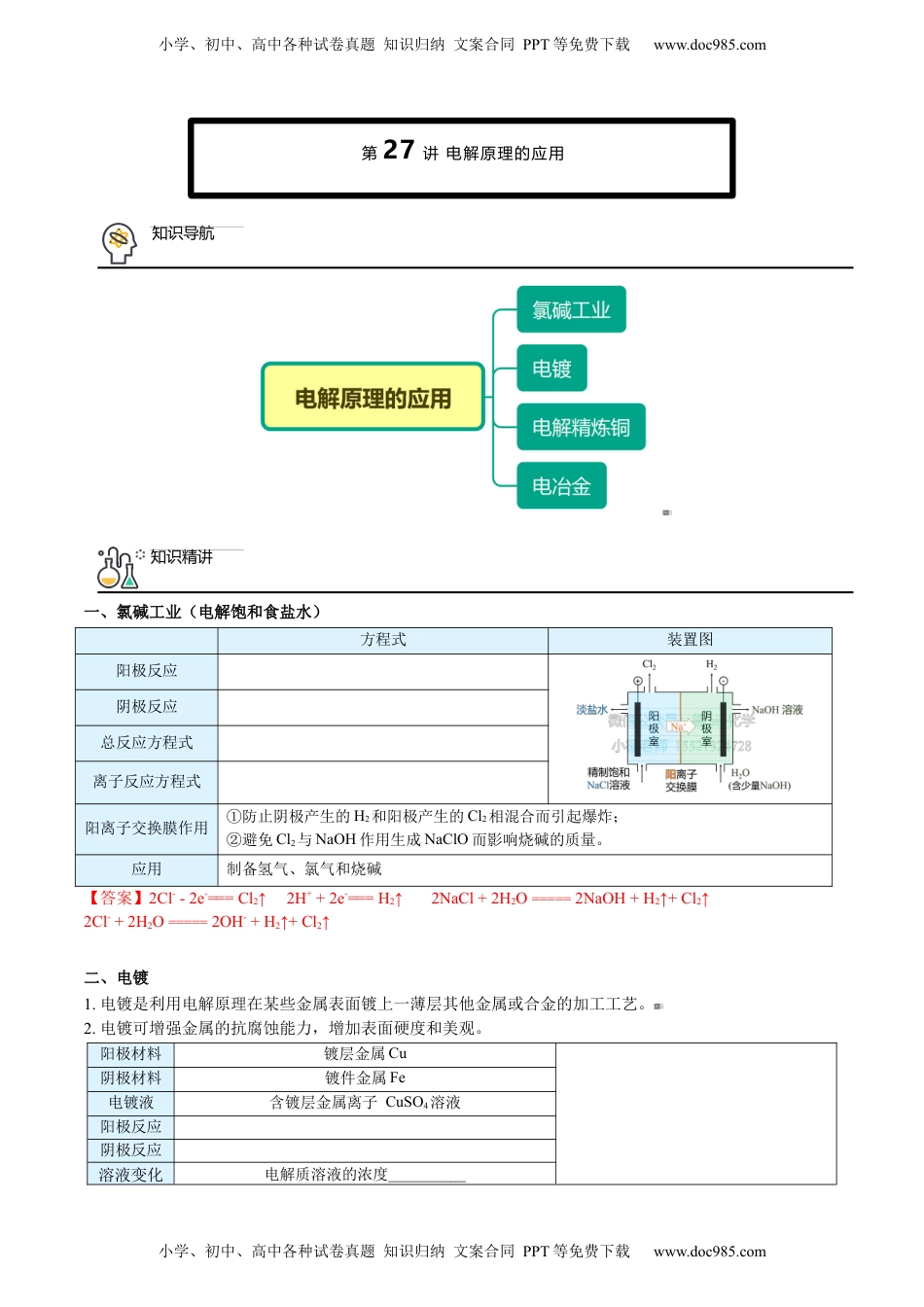
第27讲电解原理的应用知识导航知识精讲小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com一、氯碱工业(电解饱和食盐水)方程式装置图阳极反应阴极反应总反应方程式离子反应方程式阳离子交换膜作用①防止阴极产生的H2和阳极产生的Cl2相混合而引起爆炸;②避免Cl2与NaOH作用生成NaClO而影响烧碱的质量。应用制备氢气、氯气和烧碱【答案】2Cl--2e-===Cl2↑2H++2e-===H2↑2NaCl+2H2O=====2NaOH+H2↑+Cl2↑2Cl-+2H2O=====2OH-+H2↑+Cl2↑二、电镀1.电镀是利用电解原理在某些金属表面镀上一薄层其他金属或合金的加工工艺。2.电镀可增强金属的抗腐蚀能力,增加表面硬度和美观。阳极材料镀层金属Cu阴极材料镀件金属Fe电镀液含镀层金属离子CuSO4溶液阳极反应阴极反应溶液变化电解质溶液的浓度__________小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com点对训练小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com【答案】Cu-2e-===Cu2+Cu2++2e-===Cu保持不变三、电解精炼铜电解精炼粗铜时,以待精炼的铜(含Zn、Fe、Ni、Ag、Au等)作阳极,用CuSO4溶液作电解质溶液,可得含铜量为99.95%~99.98%的电解铜。阳极材料粗铜(含Zn、Fe、Ni、Ag、Au等)阴极材料纯铜阳极反应阴极反应“阳极泥”Ag、Au等金属杂质失电子能力弱,会以单质形式沉积,形成“阳极泥”。溶液变化①电解质溶液的Cu2+浓度_______②引入了Zn2+、Fe2+、Ni2+等杂质,需定时除去【答案】Zn-2e-===Zn2+Fe-2e-===Fe2+Ni-2e—===Ni2+Cu-2e-===Cu2+Cu2++2e-===Cu减小四、电冶金电冶金的本质是使矿石中的金属离子获得电子变成金属单质的过程:Mn++ne-===M电解熔融氯化钠制取金属钠方程式阳极阴极总反应【答案】2Cl--2e-===Cl2↑2Na++2e-===2Na2NaCl(熔融)=====2Na+Cl2↑题型一:氯碱工业小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com【变1】(2019·吉林·长春外国语学校高二期末)如图所示是用石墨和铁作电极电解饱和食盐水的装置,请填空:(1)X的电极反应式为:___________________________________,Y极的电极材料是_______________。(2)某同学在实验时误将两种电极材料接反,导致X极上未收集到预期产物,一段时间后又将两极的连接方式纠正过来,发现X极附近出现了白色沉淀,此沉淀是________(填化学式),其形成原因是:___________________________________。(3)工业上电解饱和食盐水的方法之一是将两个电极室用离子交换膜隔开(如图所示),其目的是_____________,阳极室(A处)加入________,离子交换膜只许________通过。【答案】2Cl--2e-===Cl2↑FeFe(OH)2铁作阳极时被氧化为Fe2+,纠正错误后,这一端又变为阴极,2H++2e-===H2↑,生成的OH-与Fe2+结合成Fe(OH)2防止H2与Cl2混合发生爆炸,防止Cl2与NaOH反应生成NaClO,使NaOH不纯饱和食盐水Na+【解析】【分析】(1)X与电源正极相连应为阳极,Y与电源负极相连应为阴极;(2)将两种电极材料接反,铁作阳极时被氧化为Fe2+,生成的OH-与Fe2+结合成Fe(OH)2;(3)将两个极室用离子交换膜隔开,其目的是防止H2与Cl2混合爆炸,防止Cl2与NaOH溶液反应生成NaClO使NaOH溶液不纯;阳极上氯离子失电子生成氯气,所以阳极室加入的是饱和食盐水;阴极室加入的是水或稀的氢氧化钠溶液,所以离子交换膜只许Na+离子通过。【详解】(1)由图可知X与电源正极相连应为阳极,电极反应式:2Cl--2e-=Cl2↑,电极材料为石墨,则Y极电极材料为Fe;故答案为2Cl--2e-=Cl2↑,Fe。(2)将两种电极材料接反,铁作阳极时被氧化为Fe2+,纠正错误后,这一端又变为阴极,2H++2e-===H2↑,生成的OH-与Fe2+结合成Fe(OH)2,故答案为Fe(OH)2;铁作阳极时被氧化为Fe2+,纠正错误后,这一端又变为阴极,2H++2e-===H2↑,生成的OH-与Fe2+结合成Fe(OH)2。(3)工业上电解饱和食盐水的方法之一,是将两个极室用离子交换膜隔开,其目的是防止H2与Cl2混合爆小学、初中、高中各种...






















发表评论取消回复