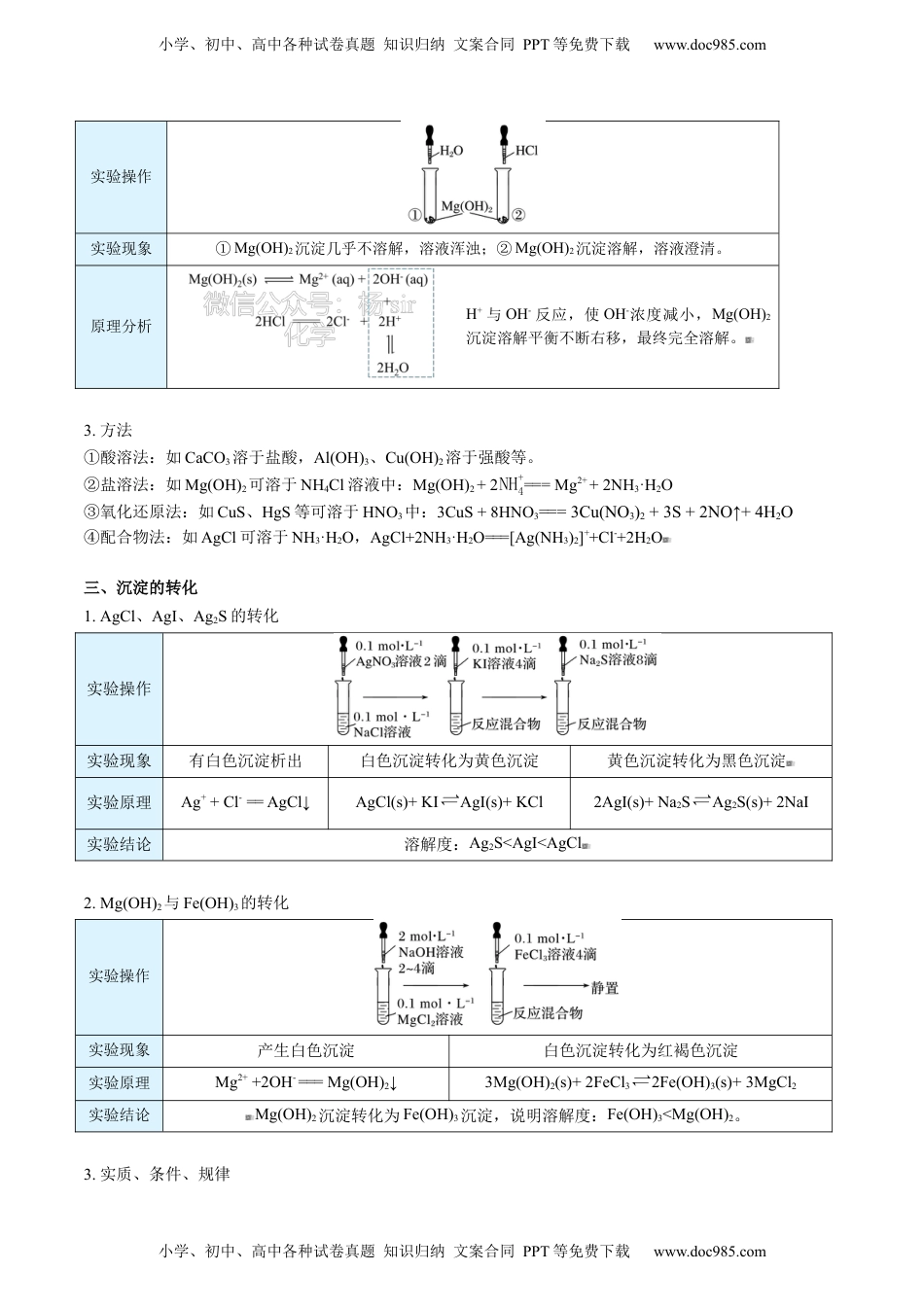
第22讲沉淀溶解平衡的应用知航识导知精识讲小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com一、沉淀的生成1.应用在无机物的制备和提纯、废水处理等领域,常利用生成沉淀来达到分离或除去某些离子的目的。2.方法方法实例操作及原理调节pH法除去NH4Cl中的FeCl3溶于水,加氨水调节pH:Fe3++3NH3·H2O===Fe(OH)3↓+3NH4+除去CuCl2中的FeCl3加入Cu(OH)2或CuO,①Fe3++3H2O⇌Fe(OH)3+3H+②Cu(OH)2+2H+===Cu2++2H2OCuO+2H+===Cu2++2H2O沉淀剂法除去废水中的Hg2+加入Na2S:S2-+Hg2+===HgS↓除去废水中的Cu2+通入H2S:H2S+Cu2+===CuS↓+2H+二、沉淀的溶解1.原理根据平衡移动原理,对于在水中难溶的电解质,如果能设法不断地移去平衡体系中的相应离子,使平衡向沉淀溶解的方向移动,就可以使沉淀溶解。2.Mg(OH)2沉淀溶解实验小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com实验操作实验现象①Mg(OH)2沉淀几乎不溶解,溶液浑浊;②Mg(OH)2沉淀溶解,溶液澄清。原理分析H+与OH-反应,使OH-浓度减小,Mg(OH)2沉淀溶解平衡不断右移,最终完全溶解。3.方法①酸溶法:如CaCO3溶于盐酸,Al(OH)3、Cu(OH)2溶于强酸等。②盐溶法:如Mg(OH)2可溶于NH4Cl溶液中:Mg(OH)2+2NH4+===Mg2++2NH3·H2O③氧化还原法:如CuS、HgS等可溶于HNO3中:3CuS+8HNO3===3Cu(NO3)2+3S+2NO↑+4H2O④配合物法:如AgCl可溶于NH3·H2O,AgCl+2NH3·H2O===[Ag(NH3)2]++Cl-+2H2O三、沉淀的转化1.AgCl、AgI、Ag2S的转化实验操作实验现象有白色沉淀析出白色沉淀转化为黄色沉淀黄色沉淀转化为黑色沉淀实验原理Ag++Cl-==AgCl↓AgCl(s)+KI⇌AgI(s)+KCl2AgI(s)+Na2S⇌Ag2S(s)+2NaI实验结论溶解度:Ag2S<AgI<AgCl2.Mg(OH)2与Fe(OH)3的转化实验操作实验现象产生白色沉淀白色沉淀转化为红褐色沉淀实验原理Mg2++2OH-===Mg(OH)2↓3Mg(OH)2(s)+2FeCl3⇌2Fe(OH)3(s)+3MgCl2实验结论Mg(OH)2沉淀转化为Fe(OH)3沉淀,说明溶解度:Fe(OH)3<Mg(OH)2。3.实质、条件、规律小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com氧化、淋滤渗透、遇闪锌矿(ZnS)和方铅矿(PbS)点对训练小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com①实质:沉淀溶解平衡的移动。②条件:两种沉淀的溶解度不同。②规律:溶解度小的沉淀转化为溶解度更小的沉淀容易实现,溶解度相差越大,转化越容易。4.沉淀转化的应用(1)锅炉除水垢(含有CaSO4)①操作:先加Na2CO3溶液,再加稀盐酸②原理:CaSO4(s)+Na2CO3⇌CaCO3(s)+Na2SO4CaCO3+2HCl===CaCl2+H2O+CO2↑(2)自然界中矿物的转化原生铜的硫化物CuSO4溶液铜蓝(CuS)CuSO4(aq)+ZnS(s)⇌CuS(s)+ZnSO4(aq);CuSO4(aq)+PbS(s)⇌CuS(s)+PbSO4(s)(3)氟化物预防龋齿①牙齿表面的釉质层,只要成分是难溶的羟基磷灰石[Ca5(PO4)3(OH)]。②口腔中的有机酸使釉质层溶解:Ca5(PO4)3(OH)+4H+===5Ca2++3HPO42-+H2O③氟离子能与羟基磷灰石反应,生成溶解度更小的氟磷灰石,更能抵抗酸的腐蚀:Ca5(PO4)3(OH)(s)+F-(aq)⇌Ca5(PO4)3F(s)+OH-(aq)题型一:沉淀的生成与溶解【变1-1】(2020·贵州·高二学业考试)已知几种难溶电解质的溶度积常数Ksp(25℃)如下:难溶电解质ZnSCuSHgSKsp向100mL含、和浓度均为0.01mol/L的溶液中逐滴加入0.001mol/L的溶液,下列说法正确的是A.先沉淀B.先沉淀C.先沉淀D.同时沉淀【变2-2】(2021·全国·高三专题练习)钴在硬质高温合金、催化剂等高新技术领域有广泛应用。从某炼锌厂的废渣(含Zn、Co、Fe、ZnO、SiO2等)中回收钴的一种工艺流程如图:小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com小学、初中、高中各种试卷真题知识归纳文案合同PPT等免费下载www.doc985.com相关金属离子[Co(Mn+)=0.1mol·L-1]形成氢氧化物沉淀的pH范围如表:金属离子Co2+Fe2+Fe3+Zn2+开始沉淀的pH7.156.31.56.2沉淀完全的pH9.158.32.88.2(1)若无氧化步骤,对实验的影响是_____。试剂X可以为下列物质...