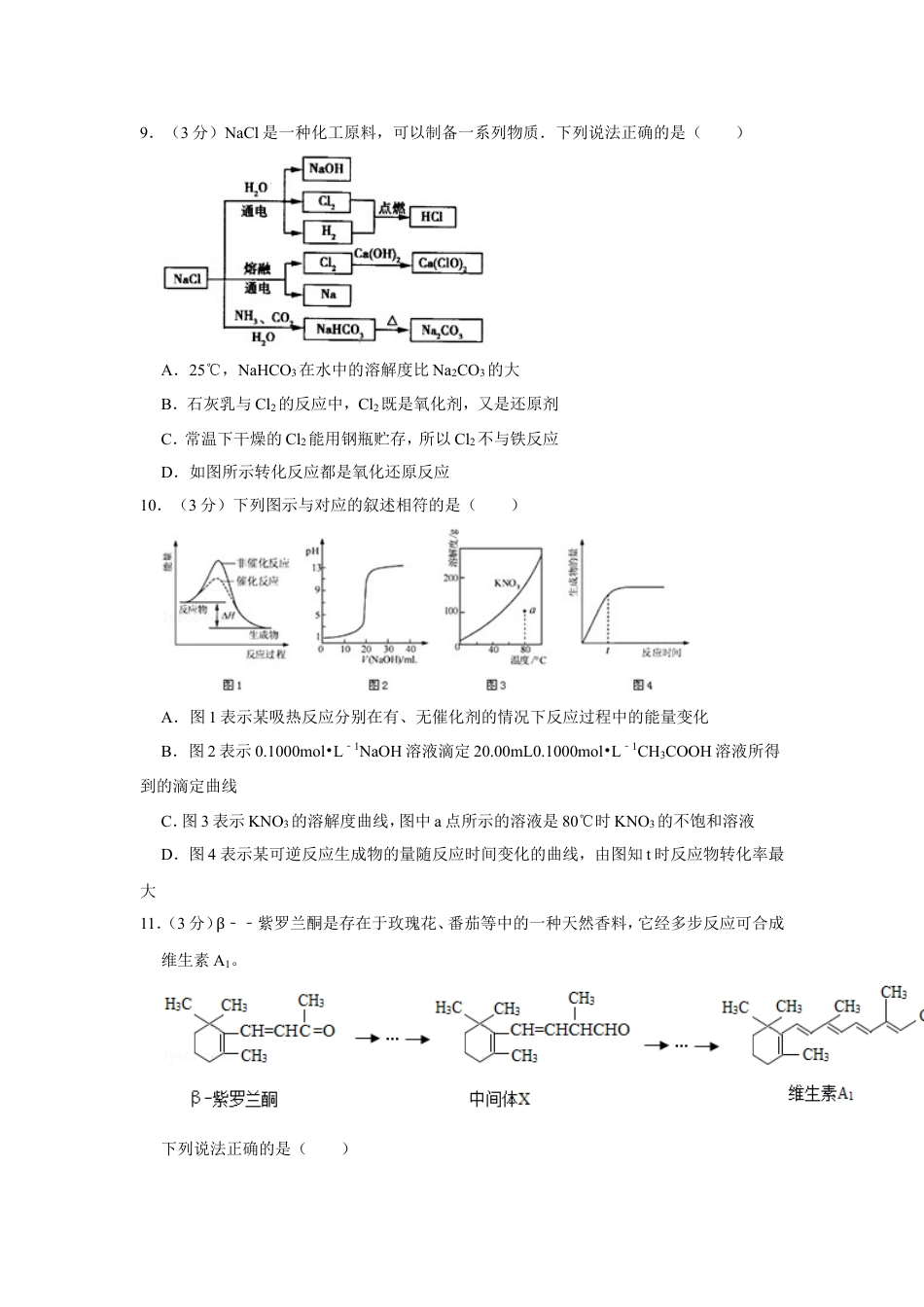
2011年江苏省高考化学试卷一、选择题1.(3分)化学与人类生活、社会可持续发展密切相关.下列措施有利于节能减排、保护环境的是()①加快化石燃料的开采与使用②研发易降解的生物农药③应用高效洁净的能源转换技术④田间焚烧秸秆⑤推广使用节能环保材料.A.①③⑤B.②③⑤C.①②④D.②④2.(3分)下列有关化学用语表示正确的是()A.N2的电子式:B.S2﹣的结构示意图:C.质子数为53,中子数为78的碘原子:D.邻羟基苯甲酸的结构简式:3.(3分)下列有关物质的性质和该性质的应用均正确的是()A.常温下浓硫酸能使铝发生钝化,可在常温下用铝制贮罐贮运浓硫酸B.二氧化硅不与任何酸反应,可用石英制造耐酸容器C.二氧化氯具有还原性,可用于自来水的杀菌消毒D.铜的金属活泼性比铁的弱,可在海轮外壳上装若干铜块以减缓其腐蚀4.(3分)常温下,下列各组离子在指定溶液中一定能大量共存的是()A.1.0mol▪L﹣1的KNO3溶液:H+、Fe2+、Cl﹣、SO42﹣B.甲基橙呈红色的溶液:NH4+、Ba2+、AlO2﹣、Cl﹣C.pH=12的溶液:K+、Na+、CH3COO﹣、Br﹣D.与铝反应产生大量氢气的溶液:Na+、K+、CO32﹣、NO3﹣5.(3分)短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示.下列说法正确的是()A.元素X与元素Z的最高正化合价之和的数值等于8B.原子半径的大小顺序为:rX>rY>rZ>rW>rQC.离子Y2﹣和Z3+的核外电子数和电子层数都不相同D.元素W的最高价氧化物对应的水化物的酸性比Q的强6.(3分)下列表示对应化学反应的离子方程式正确的是()A.FeCl3溶液与Cu的反应:Cu+Fe3+═Cu2++Fe2+B.NO2与水的反应:3NO2+H2O═2NO3﹣+NO+2H+C.醋酸溶液与水垢中的CaCO3反应:CaCO3+2H+═Ca2++H2O+CO2↑D.向NaAlO2溶液中通入过量CO2:2AlO2﹣+CO2+3H2O═2Al(OH)3↓+CO32﹣7.(3分)下列有关实验原理或实验操作正确的是()A.用水湿润pH试纸测量某溶液的pHB.用量筒量取20mL0.5000mol•L﹣1H2SO4溶液于烧杯中,加水80mL,配制成0.1000mol•L﹣1H2SO4溶液C.实验室用图所示装置制取少量氨气D.实验室用图所示装置出去Cl2中的少量HCl8.(3分)设NA为阿伏加德罗常数的值。下列叙述正确的是()A.1mol甲醇中含有C﹣H键的数目为4NAB.25℃,pH=13的NaOH溶液中含有OH﹣的数目为0.1NAC.标准状况下,2.24L己烷含有分子的数目为0.1NAD.常温常压下,Na2O2与足量H2O反应,共生成0.2molO2,转移电子的数目为0.4NA9.(3分)NaCl是一种化工原料,可以制备一系列物质.下列说法正确的是()A.25℃,NaHCO3在水中的溶解度比Na2CO3的大B.石灰乳与Cl2的反应中,Cl2既是氧化剂,又是还原剂C.常温下干燥的Cl2能用钢瓶贮存,所以Cl2不与铁反应D.如图所示转化反应都是氧化还原反应10.(3分)下列图示与对应的叙述相符的是()A.图1表示某吸热反应分别在有、无催化剂的情况下反应过程中的能量变化B.图2表示0.1000mol•L﹣1NaOH溶液滴定20.00mL0.1000mol•L﹣1CH3COOH溶液所得到的滴定曲线C.图3表示KNO3的溶解度曲线,图中a点所示的溶液是80℃时KNO3的不饱和溶液D.图4表示某可逆反应生成物的量随反应时间变化的曲线,由图知t时反应物转化率最大11.(3分)β﹣﹣紫罗兰酮是存在于玫瑰花、番茄等中的一种天然香料,它经多步反应可合成维生素A1。下列说法正确的是()A.β﹣紫罗兰酮可使酸性KMnO4溶液褪色B.1mol中间体X最多能与2molH2发生加成反应C.维生素A1易溶于NaOH溶液D.β﹣﹣紫罗兰酮与中间体X互为同分异构体12.(3分)下列说法正确的是()A.一定温度下,反应MgCl2(l)=Mg(l)+Cl2(g)的△H>0,△S>0B.水解反应NH4++H2O⇌NH3•H2O+H+达到平衡后,升高温度平衡逆向移动C.铅蓄电池放电时的负极和充电时的阳极均发生还原反应D.对于反应2H2O2=2H2O+O2↑,加入MnO2或升高温度都能加快O2的生成速率13.(3分)下列有关实验原理、方法和结论都正确的是()A.向饱和FeCl3溶液中滴加过量氨水,可制取Fe(OH)3胶体B.取少量溶液X,向其中加入适量新制氯水,再加几滴KSCN溶液,溶液变红,说明X溶液中一定含有Fe2+C.室温下向苯和少量苯酚的混合溶液中加入适量NaOH溶液,振...